NORMA Oficial Mexicana NOM-133-SSA1-1995, Que establece las especificaciones sanitarias de las agujas hipodérmicas desechables.
Al margen un sello con el Escudo Nacional, que dice: Estados Unidos Mexicanos.- Secretaría de Salud.
NORMA OFICIAL MEXICANA NOM-133-SSA1-1995, QUE ESTABLECE LAS ESPECIFICACIONES SANITARIAS DE LAS AGUJAS HIPODERMICAS DESECHABLES.
FRANCISCO J. HIGUERA RAMIREZ, Director General de Insumos para la Salud, por acuerdo del Comité Consultivo Nacional de Normalización de Regulación y Fomento Sanitario, con fundamento en los artículos 39 de la Ley Orgánica de la Administración Pública Federal; 13 Apartado A fracción I, 194 fracciones I y II, 194 Bis, 195, 197, 201, 210, 212, 213, 214, 262 y demás aplicables de la Ley General de Salud; 3o. fracción XI, 38 fracción II, 40 fracciones I, V y XII, 41, 43, 52 y 62 de la Ley Federal sobre Metrología y Normalización; 2o., 8o., 9o., 18, 24 y demás aplicables del Reglamento de Insumos para la Salud; 10 fracción XII, y 20 fracción III del Reglamento Interior de la Secretaría de Salud, y
CONSIDERANDO
Que con fecha 7 de diciembre de 1995, en cumplimiento de lo previsto en el artículo 46 fracción I de la Ley Federal sobre Metrología y Normalización, la Dirección General de Insumos para la Salud presentó al Comité Consultivo Nacional de Normalización de Regulación y Fomento Sanitario, el anteproyecto de la presente Norma Oficial Mexicana.
Que con fecha 12 de agosto de 1996, en cumplimiento del acuerdo del Comité y de lo previsto en el artículo 47 fracción I de la Ley Federal sobre Metrología y Normalización, se publicó en el Diario Oficial de la Federación el proyecto de la presente Norma Oficial Mexicana, a efecto de que dentro de los siguientes noventa días naturales posteriores a dicha publicación, los interesados presentaran sus comentarios al Comité Consultivo Nacional de Normalización de Regulación y Fomento Sanitario.
Las respuestas a los comentarios recibidos por el mencionado Comité, fueron publicadas previamente a la expedición de esta Norma en el Diario Oficial de la Federación, en los términos del artículo 47 fracción III de la Ley Federal sobre Metrología y Normalización.
Que en atención a las anteriores consideraciones, contando con la aprobación del Comité Consultivo Nacional de Normalización de Regulación y Fomento Sanitario, se expide la siguiente:
NORMA OFICIAL MEXICANA NOM-133-SSA1-1995, QUE ESTABLECE LAS ESPECIFICACIONES SANITARIAS DE LAS AGUJAS HIPODERMICAS DESECHABLES
PREFACIO
Las Unidades Administrativas que participaron en la elaboración de esta Norma son: Dirección General de Insumos para la Salud, Dirección General de Control Sanitario de Bienes y Servicios, las Instituciones: Unidad de Control Técnico de Insumos del Instituto Mexicano del Seguro Social, Dirección General de Normas de la Secretaría de Comercio (SECOFI), Secretaría de la Contraloría y Desarrollo Administrativo (SECODAM), Cámara Nacional de la Industria de la Transformación (CANACINTRA): Consejo Paramédico, Cámara Nacional de la Industria Farmacéutica (CANIFARMA): Sección de Productos Auxiliares para la Salud, Escuela Nacional de Ciencias Biológicas del IPN, Escuela Superior de Medicina del IPN, Facultad de Química de la UNAM, Facultad de Medicina de la UNAM y los establecimientos: Arrow Internacional de México, S.A. de C.V., Becton Dickinson de México, S.A. de C.V., Dentilab, S.A. de C.V., Hipode, S.A., Itochu de México, S.A. de C.V., Jeripack, S.A., Laboratorios Pisa, S.A. de C.V., Prodein, S.A., Sanko Industrial, S.A. de C.V., Serral, S.A. de C.V., Terumo Medical de México, S.A. de C.V. y Wyeth-Scherwood, S.A. de C.V.
INDICE
1. Objetivo y campo de aplicación.
2. Referencias.
3. Definiciones, símbolos y abreviaturas.
4. Clasificación.
5. Especificaciones.
6. Muestreo y clasificación de defectos.
7. Métodos de prueba.
8. Envase y embalaje.
9. Concordancia con normas internacionales y mexicanas.
10. Bibliografía.
11. Observancia de la Norma.
12. Vigencia.
1. Objetivo y campo de aplicación
1.1 Objetivo.
Esta Norma establece las especificaciones sanitarias que deben cumplir las agujas hipodérmicas desechables, así como los métodos de prueba para la verificación de las mismas, excluyendo las utilizadas en catéteres intravenosos.
1.2 Campo de aplicación.
Esta Norma debe observarse en todas las industrias, laboratorios y establecimientos, dedicados al proceso de este producto en el territorio nacional.
2. Referencias
Para la correcta aplicación de esta Norma, es conveniente consultar las siguientes normas oficiales mexicanas:
NOM-008-SCFI-1993 Sistema General de Unidades de Medida.
NOM-050-SCFI-1994 Información Comercial. Disposiciones Generales para Productos.
NOM-068-SSA1-1993 Que Establece las Especificaciones Sanitarias de los Instrumentos Quirúrgicos, Materiales Metálicos de Acero Inoxidable.
3. Definiciones, símbolos y abreviaturas
3.1 Definiciones.
Para los efectos de esta Norma se entiende por:
3.1.1 Aguja hipodérmica.
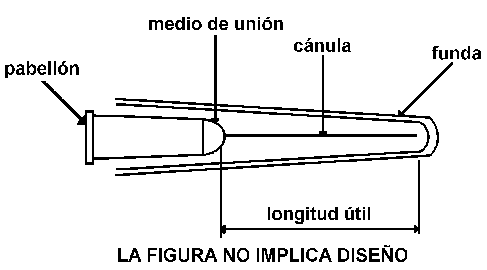
Instrumento que permite la introducción de fármacos por vía parenteral y venosa o bien la extracción de fluidos corporales. Está formada por pabellón o adaptador, cánula afilada y funda protectora. El pabellón es de plástico u otro material, el cual se ensambla por su extremo más angosto a la cánula de acero inoxidable.
3.1.2 Pabellón adaptador.
Pieza con entrada tipo Luer que permite la unión de la aguja al pivote de una jeringa, una cánula o cualquier otro instrumento médico similar.
3.1.3 Cánula de la aguja.
Tubo de acero inoxidable con punta afilada.
3.2 Símbolos y abreviaturas.
NOM Norma Oficial Mexicana
° grado
ISO International Organization for Standardization
AISI American Iron and Steel Institute
mm milímetro
% por ciento
± más o menos
x Aumento
SWG Standard Wire Gauge
Pa Pascal
atm atmósfera
kgf/cm2 kilogramo fuerza por centímetro cuadrado
Hg mercurio
Rad Radian ( 1 radian = 57.3°).
4. Clasificación
4.1 De acuerdo con el diámetro de la cánula, así como a la longitud del bisel, las agujas se clasifican como se indica en la tabla 1. La utilización del código de color por el fabricante es opcional pero puede ser solicitado por el comprador. Si se utiliza código de color debe ser el indicado en la tabla 1.
TABLA 1. CODIGO DE COLOR Y DIAMETROS DE LA CANULA
|
Código de Color (Opcional) |
Calibre SWG |
Diámetro Externo Nominal (mm) |
Diámetro Externo (mm) Mín. Máx. |
DIAMETRO |
INTERNO |
|
|
|
|
|
|
Pared Normal Mín. Máx. |
Pared Delgada Mín. Máx. |
Pared Extradelgada Mín. |
|
Amarillo |
30 |
0.30 |
0.298 0.320 |
0.133 - 0.164 |
0.165 - |
- |
|
Rojo |
29 |
0.33 |
0.324 0.351 |
0.133 - 0.189 |
0.190 - |
- |
|
Verde-Azul |
28 |
0.36 |
0.349 0.370 |
0.133 - 0.189 |
0.190 - |
- |
|
Gris medio |
27 |
0.40 |
0.400 0.420 |
0.184 - 0.240 |
0.241 - |
- |
|
Café |
26 |
0.45 |
0.440 0.470 |
0.232 - 0.291 |
0.292 - |
- |
|
Naranja |
25 |
0.50 |
0.500 0.530 |
0.232 - 0.291 |
0.292 - |
- |
|
Púrpura medio |
24 |
0.55 |
0.550 0.580 |
0.280 - 0.342 |
0.343 - |
- |
|
Azul obscuro |
23 |
0.60 |
0.600 0.650 |
0.317 - 0.359 |
0.378 - 0.399 |
0.380 |
|
Negro |
22 |
0.70 |
0.698 0.730 |
0.390 - 0.439 |
0.440 - 0.459 |
0.460 |
|
Verde obscuro |
21 |
0.80 |
0.800 0.830 |
0.490 - 0.529 |
0.530 - 0.549 |
0.550 |
|
Amarillo |
20 |
0.90 |
0.860 0.920 |
0.560 - 0.609 |
0.610 - 0.629 |
0.630 |
|
Crema |
19 |
1.10 |
1.030 1.100 |
0.648 - 0.749 |
0.730 - 0.849 |
0.850 |
|
Rosa |
18 |
1.20 |
1.200 1.300 |
0.790 - 0.909 |
0.910 - 1.040 |
1.041 |
|
Rojo violeta |
17 |
1.40 |
1.400 1.510 |
0.950 - 1.155 |
1.156 - 1.243 |
1.244 |
|
Blanco |
16 |
1.60 |
1.600 1.690 |
1.100 -1.282 |
1.283 - 1.389 |
1.390 |
|
Olivo |
15 |
1.80 |
1.750 1.900 |
1.300 -1.459 |
1.460 - 1.599 |
1.560 |
|
Verde claro |
14 |
2.10 |
1.950 2.150 |
1.500 - 1.599 |
1.500 - 1.726 |
1.727 |
5. Especificaciones
5.1
Conicidad del pabellón.El diseño del pabellón debe tener una entrada tipo Luer Hembra con una pendiente del 6%, de acuerdo con la Norma NMX-BB-87/01-1987 "Equipo para uso médico-Conectores cónicos con un 6% de conicidad Luer para jeringas, agujas y otros equipos médicos-Dimensiones y métodos de prueba Parte 1."
5.2 Bisel de la cánula.
La punta de la aguja usualmente tiene para el bisel largo un ángulo de 11° ± 2° (0.1919 rad ± 0.03491 rad) y para el bisel corto un ángulo de 17° ± 2° (0.2968 rad ± 0.03491 rad). Estas medidas son para las configuraciones que se fabrican comúnmente pero otras configuraciones diferentes pueden ser igualmente satisfactorias y no es necesario mencionar en esta Norma las dimensiones correspondientes a todas las diferentes configuraciones (ISO 7864-1993-05-15 numeral 12), pero el fabricante deberá señalar las dimensiones correspondientes a la configuración en particular.
5.3 Materiales.
Los materiales usados para la manufactura de agujas hipodérmicas, desechables, bajo condiciones normales de uso, no deben producir sustancias tóxicas y deben estar libres de pirógenos y no producir reacciones tisulares, cuando se prueba de acuerdo con el procedimiento descrito en la NMX-BB-006-1990 "Equipo para uso médico: Toxicidades, pirogenicidades y reacciones tisulares en jeringas, agujas y otros equipos similares. Métodos de prueba".
5.3.1 Pabellón.
Material plástico grado médico USP u otro material equivalente.
5.3.2 Cánula.
Debe ser de acero inoxidable austenítico correspondiente a los tipos 11, 12 y 20 de la Norma ISO-683, los cuales son equivalentes a los tipos 304, 302 y 316, respectivamente, de AISI, los cuales son indicados en la Tabla 2 y deben cumplir con las pruebas establecidas en la tabla 3.
TABLA 2. COMPOSICION QUIMICA (POR CIENTO)
|
Acero Inox. ISO-683/13 |
Acero Inox. AISI |
Carbono C Máx. |
Cromo Cr |
Molibdeno Mo |
Silicio Si Máx. |
Fósforo P Máx. |
Azufre S Máx. |
Níquel Ni |
Manganeso Mn Máx. |
Hierro Fe |
|
11 |
304 |
0.08 |
16.80 a 19.20 |
- |
1.05 |
0.050 |
0.035 |
7.85 a 11.85 |
2.04 |
Balance |
|
2 |
302 |
0.12 |
16.80 a 19.20 |
- |
1.05 |
0.050 |
0.035 |
7.90 a 10.10 |
2.04 |
Balance |
|
20 |
316 |
0.08 |
15.80 a 18.70 |
1.90 a 2.60 |
1.05 |
0.050 |
0.035 |
10.35 a 14.15 |
2.04 |
Balance |
TABLA 3. PRUEBAS DE LA CANULA
|
PARAMETRO |
ESPECIFICACION |
METODO DE PRUEBA |
|
Resistencia a la corrosión. |
Debe cumplir la especificación. |
Numeral 7.3. |
|
Resistencia a la fatiga. |
No debe presentar fisuras o fracturas. |
Numeral 7.4. |
5.3.3
Rigidez de la cánula.Debe cumplir con lo establecido en la tabla 10, de acuerdo con el procedimiento descrito en el numeral 7.8.
5.4 Acabados.
5.4.1 Pabellón.
La superficie del pabellón debe ser uniforme, libre de defectos que impidan su funcionalidad, la superficie de apoyo, de su borde circular inferior, debe ser lisa, de tal forma que exista un adecuado acoplamiento con el pivote de las jeringas para una unión hermética. Esto debe verificarse visualmente.
5.4.2 Código de Color.
El diámetro externo nominal de las agujas hipodérmicas puede identificarse rápidamente por el código de color de acuerdo con la ISO-6009 e ISO-7864, las cuales indican que el color aplica en la unidad contenedora o en el pabellón de la aguja o en la funda o vaina de la misma y debe estar en concordancia con el código de colores señalado en la tabla 1. La observación del código de color no elimina la obligación de verificar el calibre de la aguja. La utilización del código de color por el fabricante es opcional.
5.4.3 Cánula.
El acabado en toda la superficie debe ser uniforme y estar libre de rebabas, fisuras, fracturas, grietas, áreas rugosas, muescas, obstrucción, poros, corrosión a simple vista o superposición de material. La punta de la aguja debe presentar filo cortante, no debe tener punta roma deformada o sin filo. Esto debe verificarse visualmente.
Además de las características indicadas en el párrafo anterior, se requiere cualquiera de los dos tipos de acabado mencionados a continuación.
5.4.3.1 Espejo.
Las cánulas deben presentar una superficie pulida de alta reflexión. Esto se verifica visualmente, si tiene color, éste debe ser de acuerdo con el código de color de la tabla 1.
5.4.3.2 Satinado.
Las cánulas deben presentar una superficie lisa de baja reflexión.
5.5 Lubricado de la cánula.
La superficie exterior de la cánula debe ser lubricada con un lubricante de grado médico. Esto se verifica de acuerdo con el procedimiento descrito en el numeral 7.5.
5.6 Funda protectora.
Material plástico rígido o semirígido con buena resistencia mecánica para proteger la cánula contra posibles deformaciones en su manejo normal. Puede ser translúcida o pigmentada, si es en color, éste debe estar en concordancia con el código de colores indicado en la tabla 1.
5.7 Longitud útil de la cánula.
La longitud útil de la cánula debe estar de acuerdo con lo establecido en la tabla 4 y figura 1.
TABLA. 4. LONGITUD UTIL DE LA CANULA
|
DIMENSION NOMINAL (mm) |
TOLERANCIA (mm) |
|
6 a 9 |
+ 1 - 2 |
|
10 a 19 |
+ 1 - 2 |
|
20 a 38 |
+ 1.5 - 2.5 |
|
39 a 50 o mayor |
+ 1.5 - 2.5 |
5.8
Físicas, fisicoquímicas, biológicas y microbiológicas.La aguja en todas sus partes debe cumplir con las especificaciones de la tabla 5.
TABLA 5. ESPECIFICACIONES DE LA AGUJA
|
PARAMETRO |
ESPECIFICACIONES |
METODO DE PRUEBA |
|
Pirógenos. Toxicidad. Reacciones tisulares. Esterilidad. Oxido de etileno residual. Hermeticidad. Prueba rigidez. Prueba de dureza - Vickers. Adherencia entre pabellón y cánula. Evidencia de flujo. |
Libre de pirógenos. Debe ser atóxica. No debe provocar. Debe ser estéril. 25 ppm máximo. Debe cumplir la especificación. Debe cumplir la especificación. Debe cumplir la especificación. Debe cumplir la especificación. Debe cumplir la especificación. |
NMX-BB-006-1990 NMX-BB-006-1990 NMX-BB-006-1990 NMX-BB-008-1990 NMX-BB-092-1989 Numeral 7.9 Numeral 7.8 Numeral 7.12 Numeral 7.6 Numeral 7.7 |
6. Muestreo y clasificación de defectos
6.1
Muestreo.Para efectos de muestreo e inspección se recomienda aplicar la Norma Mexicana NMX-Z-12-1987 (Muestreo para la Inspección por Atributos). Conservando invioladas las muestras que presenten defectos críticos.
6.2 Clasificación de defectos.
6.2.1 Defectos críticos.
- Corrosión a simple vista.
- Muescas, rebabas, fisuras y fracturas en la cánula.
- Cánula tapada.
- Superposición de material.
- Puntas romas, deformadas o sin filo.
- Partículas extrañas o impurezas dentro del empaque primario.
- Empaque primario inadecuado, mal sellado, deteriorado, roto o abierto.
- Datos y leyendas que no correspondan al producto (empaque primario y secundario).
- Etiquetas con información ilegible o borrosa.
- Falta total de datos y leyendas (empaque primario y secundario).
- Falta de etiquetas o contraetiquetas con datos y leyendas en idioma español (empaque primario y secundario).
- Falta de alguno de los datos indicados en el empaque primario de acuerdo con lo establecido en el numeral 8.1.1.
6.2.2 Defectos mayores.
- Empaque primario sucio o manchado.
- Empaque secundario inadecuado, deteriorado, roto o abierto.
- Falta de alguno de los datos o leyendas en el empaque secundario de acuerdo con lo establecido en el numeral 8.1.2.
6.2.3 Defectos menores.
- Etiquetas y empaques con información ligeramente borrosa pero legible.
- Etiquetas deterioradas o mojadas pero con información legible y completa.
- No cumplir con otros requisitos de etiquetado indicados por los organismos oficiales.
7. Métodos de prueba
Los aparatos utilizados deben estar debidamente calibrados; todas las pruebas deben realizarse empleando disolventes y reactivos grado reactivo, agua destilada, material de vidrio de borosilicato de bajo coeficiente de expansión térmica, a menos que se indiquen otras condiciones. Utilizar un mínimo de 12 agujas para cada prueba con excepción de los métodos donde se indique el número de piezas a evaluar.
Para verificar la calidad del producto objeto de esta Norma, deben aplicarse los métodos de prueba referidos a continuación:
7.1 Inspección del acabado.
7.1.1 Procedimiento.
La superficie de las agujas debe ser inspeccionada a simple vista o con un lente de aumento de 2.5X para verificar su acabado. Evaluar 20 agujas como mínimo.
7.1.2 Interpretación.
Debe cumplir con todo lo establecido en el numeral 5.4.
7.2 Análisis químico del material.
7.2.1 Procedimiento.
Debe efectuarse como mínimo con 20 agujas de acuerdo con los métodos establecidos en la NMX-B-067-1991 "Industria Siderúrgica. Recomendación para el Análisis Químico de Metales por Métodos Fotométricos".
7.2.2 Interpretación.
Los porcentajes obtenidos deben estar dentro de los valores especificados en la tabla 2.
7.3 Resistencia a la corrosión (ácido cítrico).
7.3.1 Procedimiento.
Desprender la cánula del pabellón de la aguja. Sumergirla durante 5 horas en un recipiente de vidrio, el cual contiene una solución al 10% de ácido cítrico a temperatura ambiente. Posteriormente retirar de la solución, sumergirla en agua destilada y hervirla durante 30 minutos. Permitir el enfriamiento del agua y de la cánula sumergida y dejar a temperatura ambiente durante 48 horas. Transcurrido este tiempo, retirar la cánula del agua y secarla por evaporación para su inspección.
Evaluar 5 agujas como mínimo.
7.3.2 Interpretación.
La cánula no debe presentar indicios de corrosión sobre su superficie.
7.4 Resistencia a la fatiga de la cánula.
7.4.1 Procedimiento.
Desprender la cánula del pabellón. Sujetar firmemente la cánula por uno de los extremos.
Aplicar a la distancia que se indica en la tabla 6, una fuerza suficiente para flexionar la cánula, un ángulo de 25° ± 2° (0.4363 Rad ± 0.0349 Rad) sobre su eje longitudinal, efectuar 20 ciclos. Posteriormente invertir el sentido de la fuerza y repetir la misma operación de flexión con 20 ciclos.
Evaluar 5 agujas como mínimo.
7.4.2 Interpretación.
Al examinar a simple vista la cánula, no debe haber fisuras o fracturas.
TABLA 6. RESISTENCIA A LA FATIGA Dimensiones en mm
|
CALIBRE |
DIAMETRO EXTERNO NOMINAL (mm) |
DISTANCIA ENTRE EL SOPORTE RIGIDO Y EL PUNTO DE APLICACION DE LA FUERZA DE FLEXION (± 0.1 mm) |
|
30 29 28 27 26 25 24 23 22 21 20 19 18 17 16 15 14 |
0.30 0.33 0.36 0.40 0.45 0.50 0.55 0.60 0.70 0.80 0.90 1.10 1.20 1.40 1.60 1.80 2.10 |
8 8 8 8 10 10 12.5 15 17.5 20.0 25.0 27.5 30 31.5 31.5 31.5 31.5 |
7.5
Verificación del lubricado de la superficie exterior de la cánula.7.5.1 Procedimiento.
Tomar 5 agujas y sumergirlas en un recipiente con harina o con polvo de talco, hasta que el pabellón alcance la superficie de la harina o polvo de talco. Retirarlas inmediatamente y verificar visualmente.
7.5.2 Interpretación.
La superficie exterior de la cánula debe tener adherida uniformemente una capa de harina o polvo de talco.
7.6 Adherencia entre el pabellón y la cánula.
7.6.1 Procedimiento.
Sujetar firmemente la aguja por los extremos, considerando su diámetro externo nominal, aplicar la fuerza de tensión correspondiente, indicada en la tabla 7.
Evaluar 5 agujas como mínimo.
7.6.2 Interpretación.
Al examinar a simple vista la aguja, no debe existir desplazamiento, fisuras o fracturas entre el pabellón y la cánula.
TABLA 7. ADHERENCIA ENTRE EL PABELLON Y LA CANULA
|
CALIBRE SWG |
DIAMETRO EXTERNO NOMINAL (mm) |
FUERZA DE TENSION MINIMA N (± 0.1) |
|
30 29 28 27 26 25 24 23 22 21 20 19 18 17 16 15 14 |
0.30 0.33 0.36 0.40 0.45 0.50 0.55 0.60 0.70 0.80 0.90 1.10 1.20 1.40 1.60 1.80 2.10 |
22 22 22 22 22 22 34 34 40 44 54 69 69 69 69 69 69 |
7.7
Evidencia de flujo.7.7.1 Procedimiento.
De acuerdo con el diámetro externo nominal de la cánula seleccionar el estilete adecuado de los indicados en la tabla 8 y hacerlo pasar a través de la cánula, con el objeto de verificar que no esté obstruida.
Posteriormente, retirar el estilete y hacer pasar por la cánula un flujo de agua, cuyo porcentaje no sea menor al 80% del flujo que pasa por una cánula de diámetro y longitud equivalente. La presión de agua durante la prueba no debe exceder de 1 x 105 Pa (1 atm).
Evaluar 5 agujas como mínimo.
7.7.2 Interpretación.
El estilete debe pasar libremente por la cánula o el flujo de agua debe salir libremente por la punta de la cánula.
TABLA 8. ESTILETES PARA LA PRUEBA DE EVIDENCIA DE FLUJO DIMENSIONES EN mm
|
CALIBRE (SWG) |
DIAMETRO EXTERNO NOMINAL (mm) |
DIAMETRO DEL ESTILETE (mm) |
|
30 29 28 27 26 25 24 23 22 21 20 19 18 17 16 15 14 |
0.30 0.33 0.36 0.40 0.45 0.50 0.55 0.60 0.70 0.80 0.90 1.10 1.20 1.40 1.60 1.80 2.10 |
0.11 0.11 0.11 0.15 0.18 0.18 0.22 0.25 0.30 0.40 0.48 0.58 0.70 0.76 0.88 1.04 1.20 |
7.8
Rigidez de la cánula.7.8.1 Procedimiento. (De acuerdo con el método establecido en la Norma ISO 9226).
Desprender, si es necesario, la cánula del pabellón y de acuerdo con su diámetro nominal, aplicarle una fuerza o carga central entre dos soportes colocados a la distancia especificada en la tabla 9.
Evaluar 5 agujas como mínimo.
7.8.2 Interpretación.
La cánula no debe presentar otro grado de deflexión mayor al especificado en la tabla 9.
7.9 Hermeticidad.
7.9.1 Procedimiento.
Debe efectuarse de acuerdo con lo indicado en la Norma NMX-BB-047-1976. Determinación de la hermeticidad en agujas desechables, bloquear la punta de la aguja, ensamblarla con el cono Luer maestro, aplicar presión hidráulica de 2.8 kgf/cm² durante 5 segundos.
Evaluar 5 agujas como mínimo.
7.9.2 Interpretación.
No deben presentarse fugas de agua en la unión del pabellón y el cono Luer maestro o en la unión del pabellón con la cánula.
7.10 Dimensiones.
Debe efectuarse en 12 piezas como mínimo.
7.10.1 Interpretación.
Los valores obtenidos deben estar en concordancia con lo especificado en las tablas 1, 2 y 4.
TABLA 9. RIGIDEZ DE LA CANULA
|
CALIBRE SWG |
DIAM. EXTERNO NOMINAL (mm) |
CANULA PARED NORMAL |
CANULA PARED DELGADA |
CANULA PARED EXTRADELGADA |
|||||||
|
|
|
DISTANCIA (mm) ± 0.1 |
CARGA NEWTON ± 0.1 |
DEFLEXION Máx. (mm) |
DISTANCIA (mm) ± 0.1 |
CARGA NEWTON ± 0.1 |
DEFLEXION Máx. (mm) |
DISTANCIA (mm) ± 0.1 |
CARGA NEWTON ± 0.1 |
DEFLEXION Máx. (mm) |
|
|
30 29 28 27 26 25 24 23 22 21 20 19 18 17 16 15 14 |
0.3 0.33 0.36 0.40 0.45 0.50 0.55 0.60 0.70 0.80 0.90 1.10 1.20 1.40 1.60 1.80 2.10 |
5.0 5.0 5.0 9.5 10.0 10.0 10.0 12.5 15.0 15.0 17.5 25.0 25.0 25.0 25.0 25.0 30.0 |
5.5 5.5 5.5 5.5 6.0 7.0 10.0 10.0 10.0 15.0 15.0 10.0 20.0 22.0 22.0 25.0 40.0 |
0.40 0.32 0.25 0.60 0.58 0.38 0.50 0.40 0.45 0.41 0.48 0.45 0.45 0.45 0.25 0.35 0.40 |
5.0 5.0 5.0 7.5 10.0 10.0 10.0 12.5 15.0 15.0 17.5 25.0 25.0 25.0 26.0 25.0 30.0 |
5.5 5.5 5.5 5.5 5.5 7.0 10.0 10.0 10.0 15.0 15.0 10.0 20.0 22.0 22.0 25.0 40.0 |
0.45 0.37 0.30 0.65 0.61 0.43 0.55 0.45 0.50 0.50 0.55 0.55 0.55 0.55 0.30 0.45 0.50 |
- - - - - - - 12.5 15.0 15.0 15.0 25.0 25.0 25.0 25.0 25.0 25.0 |
- - - - - - - 10 10 10 10 10 10 10 22 22 22 |
- - - - - - - 0.50 0.55 0.55 0.55 0.65 0.65 0.55 0.34 0.34 0.34 |
|
7.11
Sellado del empaque primario.7.11.1 Procedimiento.
Las agujas en su empaque primario se introducen en una jarra de vacío, aplicando un vacío absoluto de 304.8 mm Hg (12 pulgadas de mercurio). Si alguna parte del empaque es porosa (no tenga recubrimiento plástico) debe cubrirse con glicerina pura.
Evaluar 5 agujas como mínimo.
7.11.2 Interpretación.
Los empaques deben inflarse, lo que indica un sellado correcto. Los empaques que no se inflen o se abran por el área del sellado durante la prueba, evidencian un sellado inadecuado.
7.12 Dureza.
7.12.1 Procedimiento.
Verificar de acuerdo con el método establecido en la Norma Mexicana NMX-B-118-1974 Determinación de Dureza Vickers en Materiales Metálicos.
7.12.2 Interpretación.
El promedio obtenido de las lecturas debe ser de 343 HV a 485 HV (microdureza vickers) (35-48 Rockwell C).
8. Empaque y embalaje
8.1 Empaque.
Los empaques del producto deben reunir las especificaciones señaladas en los artículos 20 y 22 del Reglamento de Insumos para la Salud.
El tipo y la calidad del empaque debe proteger el producto y resistir las condiciones normales de manejo, transporte y almacenamiento en los diferentes climas del país.
8.1.1 Empaque primario.
Individual, hermético, que preserve la esterilidad. Con una cara transparente o translúcida.
Deben llevar impresos en el empaque o en una etiqueta en forma legible los siguientes datos en español, de acuerdo con la Ley General de Salud y el Reglamento de Insumos para la Salud.
- Nombre del producto.
- Marca o razón social del fabricante y de ser posible el domicilio.
- Calibre y longitud nominal en el Sistema Internacional de Unidades.
- Estéril.
- Desechable o para usarse una sola vez.
- No tóxica.
- Libre de pirógenos.
- Número de registro otorgado por la SSA.
- Número de lote.
- Hecho en México o país de origen.
- Si el tamaño del empaque primario no permite adherir una contraetiqueta sin cubrir los datos originales, la contraetiqueta se deberá colocar en el empaque secundario, y
- Los demás que señale el Reglamento de Insumos para la Salud.
8.1.2
Empaque secundario.Caja de cartón u otro material que proteja al producto durante su transporte y almacenamiento.
Además de lo indicado en 8.1.1, debe llevar impresos en forma legible en el empaque secundario o en una etiqueta los siguientes datos en español:
- Razón social y domicilio del fabricante.
- Razón social y domicilio comercial del distribuidor autorizado cuando el producto sea de importación.
- No se garantiza la esterilidad del producto en caso de que el envase tenga señales de haber sufrido ruptura previa.
- Este producto deberá desecharse después del uso, en forma adecuada para evitar punciones accidentales, y
- Los demás que señale el Reglamento de Insumos para la Salud.
8.2
Embalaje.Caja de cartón corrugado con una resistencia mínima de 1.07 MPa (11 kgf/cm2) o algún otro material con propiedades similares.
8.3 Almacenamiento.
El producto objeto de esta Norma, debe almacenarse en locales cubiertos, protegidos de la lluvia, de la exposición directa a los rayos del sol, lejos de fuentes emisoras de calor o vapores, en condiciones de estiba que aseguren la integridad del producto.
9. Concordancia con normas internacionales y mexicanas
Esta Norma concuerda parcialmente con las normas ISO-6009-1992 e ISO-7864-1993.
10. Bibliografía
|
10.1 |
Ley General de Salud, Título Décimo Segundo, Capítulo I, artículos 209 y 210, 1992. |
|
10.2 |
Ley Federal sobre Metrología y Normalización, 1993. |
|
10.3 |
Reglamento de Insumos para la Salud. |
|
10.4 |
Farmacopea de los Estados Unidos Mexicanos, Sexta Edición, 1994. |
|
10.5 NMX-BB-092-1989 |
Industria del Plástico-Equipo para uso médico-Contenido de óxido de etileno residual-Método de prueba. |
|
10.6 NMX-BB-047-1976 |
Determinación de la hermeticidad en agujas desechables. |
|
10.7 NMX-BB-044-1976 |
Determinación de esterilidad en agujas hipodérmicas desechables. |
|
10.8 NMX-BB-087/01-1987 |
Equipo para uso médico-Conectores cónicos con un 6% de conicidad Luer para jeringas, agujas y otros equipos médicos-Dimensiones y métodos de prueba Parte 1. |
|
10.9 NMX-BB-008-1990 |
Equipo para uso médico-Esterilidad-Método de prueba. |
|
10.10 NMX-BB-042-1976 |
Determinación de toxicidad, pirogenicidad y reacciones tisulares en agujas hipodérmicas desechables. |
|
10.11 NMX-B-001-1988 |
Métodos de Análisis Químico para determinar la composición de Aceros y Fundiciones. |
|
10.12 NMX-B-078-1978 |
Métodos de Análisis Fotométrico para determinar la Composición Química de Aceros y Fundiciones. |
|
10.13 NMX-BB-046-1976 |
Determinación de la Resistencia a la Corrosión en Agujas Hipodérmicas Desechables. |
|
10.14 NMX-BB-083-1981 |
Industria Farmacéutica Materiales para uso Médico-Agujas Hipodérmicas reusables. Especificaciones. |
|
10.15 NMX-BB-006-1990 |
Equipo para uso médico: Toxicidades, pirogenicidades y reacciones tisulares en jeringas, agujas y otros equipos similares. Métodos de prueba. |
|
10.16 NMX-BB-045-1976 |
Industria Farmacéutica. Materiales para uso médico: Agujas hipodérmicas estériles para usarse una sola vez. Especificaciones. |
|
10.17 ISO-7864-1993 |
Sterile hypodermic needles for single use. |
|
10.18 |
Cuadro Básico de Materiales, Reactivos y Medios de Diagnóstico para Laboratorios del Sector Salud de 1986. |
|
10.19 ISO-6009-1992 |
Hypodermic needles for single use-Colour coding for identification. |
|
10.20 ISO-10993-1-1992 |
Biological evolution of medical devices. Part 1, Guidance on selection of tests. |
|
10.21 NMX-Z-12-1987 |
Muestreo para la Inspección de Atributos. |
11. Observancia de la Norma
La vigilancia del cumplimiento de la presente Norma corresponde a la Secretaría de Salud, cuyo personal realizará la verificación y la vigilancia que sean necesarias.
12. Vigencia
La presente Norma entrará en vigor con carácter obligatorio al día siguiente de su publicación en el Diario Oficial de la Federación.
Atentamente
Sufragio Efectivo. No Relección.
México, D.F., a 19 de octubre de 1998.- El Director General de Insumos para la Salud, Francisco J. Higuera Ramírez.- Rúbrica.

Fecha de publicación: 29 de cotubre de 1998
Si quiere obtener una copia del texto completo, presione aquí ![]()